歯周病治療
位相差顕微鏡による歯周病細菌検査
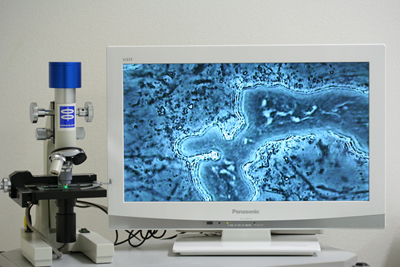
位相差顕微鏡検査とは?
口腔内には500~700種類の細菌が生息しています。
こうした口腔内細菌が歯周病や虫歯といった歯を失う原因となっているのです。
当医院では 位相差顕微鏡 を使用して口腔内細菌の種類や量 等を観察します。
口腔内に存在する細菌により除菌方法も変わってきますので 患者様にあった除菌方法で治療を行います。
歯周病を起こす細菌は口腔常在菌(健康な状態であっても存在する細菌)なので、歯周病治療を行ったとしても全ての歯周病細菌を「ゼロ」にはできませんが、極力数減らすことが歯周病活動を抑えたり、再発を少なくすることにつながります。
以下は位相差顕微鏡で見た歯周病細菌の動画(YouTube)です。
上側が初診時の深い歯周ポケット内部に生息するスピロヘータ(らせん菌)という細菌です。
らせん状の動いているのがスピロヘータです。
このような細菌が大量に存在することは良いことではありません。
下側が治療終了後です。
スピロヘータの減少が認められます。
検査方法
1. 歯周ポケットからプラーク(汚れ)を採取する
※ 歯周ポケットについては以下を参考にして下さい。 歯周ポケット検査(歯周病の基本的な検査)
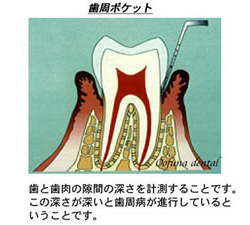
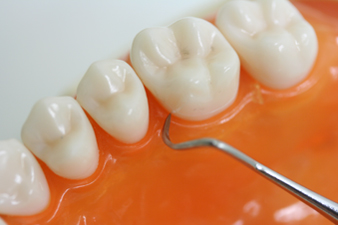
実際の検査では滅菌したペーパーポイントという物を使用します。
2. プラーク(汚れ)をプレパラート(透明のガラス板)に置く
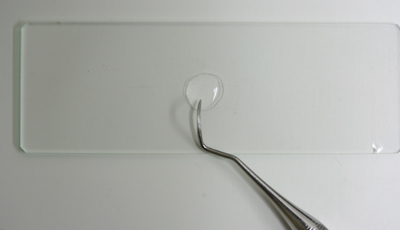
3. 位相差顕微鏡に設置する

4. 位相差顕微鏡に接続されたモニターで細菌の動きをリアルタイムで観察することができます
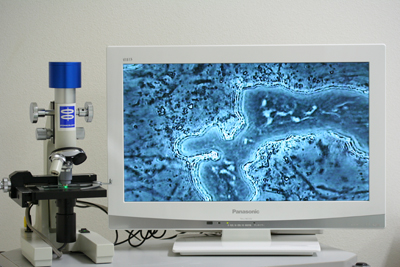
プラーク(汚れ)の採取からモニターで観察するまで1分もかかりません。
もちろん痛みもありません。
非常に簡単な検査です。
位相差顕微鏡検査 治療費
歯周病ポケット検査と一緒に行いますので、位相差顕微鏡治療費自体は無料です。
どんな細菌が見えるのか?
スピロヘータ
歯周病が進行した歯周ポケット内部では大量に認められるため、歯周病の活動度や重症度と関連される細菌です。
治療後にもこの細菌の割合が高いと再発が早いとされ、この細菌の水準が治療効果の指標として有効とされています。
ここまでの内容で位相差顕微鏡についての大まかなところはご理解されたと思います。
以下の内容は、「歯周病についてさらに知りたい!」という方のために相当難しい内容になりますが、口腔内細菌についてまとめてみましたのでご興味のある方は是非参考にされて下さい。
全部をみると相当な時間(20分程度はかかります)がかかりますが、これを読み終えると相当な「歯周病ツウ」になりますよ!
1. 私達の身体は細菌だらけ!
人間は一生の中で無菌の状態でいられるのは胎内で過ごす期間だけです。
出生するとすぐに細菌感染を起こし、生体の各所で菌の増殖が始まります。
一度細菌感染した部位は一生排除されずに定着するものも少なくないのです。
つまり私達の生体は細菌と共存している状態なのです。
2. 歯周病は感染症!
歯周病細菌はどこから感染すると思いますか?
例えば、侵襲性歯周炎(しんしゅうせいししゅうえん)の原因菌とされるAa菌(Aggregatibacter actinomycetemcomitans)は、大人から大人へと感染することはなく、まだ永久歯が生えそろわない10歳頃に大人から子供へ感染することが研究により分かっています。
※ Slos J:Scand J Dent Res,1976
これは子供の口腔内はまだ細菌のグループが安定していないため、外来から感染を起こします。
また、抗生剤を長期服用していた場合などは、口腔内の健康な細菌グループがいったんいなくなるため、新たに細菌の環境がそろう前に細菌に感染する可能性があります。
※ 細菌の名称はよく変わります。上記は2011年時点での名称です。
旧名は、Actinobacillus actinomycetemcomitansです。
※ 1999年以前に思春期前歯肉炎、若年性歯周炎、急速進行性歯周炎と呼ばれていたものをまとめて侵襲性歯周炎と分類しています。
その他の歯周病細菌についても夫婦間や親子間で感染していることが多くの研究で明らかにされています。
※ Greenstein G, et al:J Periodontol,1997
※ Petit M D A,et al:J Periodont Res,1993
唾液を介した感染が主なルートであれば、歯周病治療後の再感染を防止したり、歯周病細菌を持っている人がそうでない人に移さないようにすることは重要です。
歯周病治療を行う場合には、ご本人の治療を行うだけでなく、生活を共にしている家族全ての人の治療が必要ということになります。
3. 口腔内には細菌がいっぱい!
人間の身体にはさまざまな部位で細菌が生息しています。
口腔内に生存する細菌の種類は500~700種類と言われています。
口腔内に存在するデンタルプラーク中の細菌はものすごい数です。
デンタルプラーク1mg当たりの細菌の数は1億個も存在します。
デンタルプラークは細菌の塊なのです。
「えーそんなに細菌がいるの?」
と思われるかと思います。
しかし、口腔内に生息する細菌が全て問題なのではありません。
正常細菌叢(せいじょうさいきんそう)と言われる細菌は、健康な身体に住み着く細菌です。
これらの正常細菌叢は、外部からの絶えまなく侵入してくる病原微生物からの攻撃を防御しているのです。
細菌が存在することは決して悪いことではないのです。
外出から帰ってきたり、食事の前に手を洗うことは非常に有効です。
しかし、これにより細菌がいなくなるわけではありません。
その理由について解説します。
例えば、皮膚に存在する常在細菌は、1cm2当たり10,000個存在しています。
これらの常在細菌は、適切な手洗い(水、石けん等の使用)で90%以上除去されます。
しかし、除去される細菌は表層のみであり、毛嚢(もうのう)や汗腺(かんせん)の深部に定着している細菌は容易に除去できないため、数時間経つとこれらの細菌が増殖し元の状態に戻ってしまいます。
ただし、これが悪いわけではありません。
常在細菌は常にバランスを保っており、特定の細菌が増えないようにコントロールされているのです。
しかし、衛生面を極度に意識し、過剰な消毒を繰り返すことによりそのバランスが崩れて悪影響を及ぼすこともあります。
口腔内の細菌もそうです。
先程説明したように口腔内の歯垢(しこう)には、1mg当たりの細菌の数は1億個も存在します。
唾液には、1ml当たり105~109個存在しています。
これは正常な状態なのです。
問題となるのは、細菌のバランスと種類なのです。
4. 好気性菌と嫌気性菌とは?
口腔内の細菌を理解するためには、好気性菌 と 嫌気性菌 という2つの細菌を知ることが必要です。
口腔内には大きく分けて好気性菌(こうきせいきん) と 嫌気性菌(けんきせいきん)が存在します。
好気性菌は、酸素が存在する部位でのみ生きることが可能な細菌です。
嫌気性菌は、酸素が存在する部位では生きるのが困難な細菌です。
先程デンタルプラークには 多くの細菌が生息していると説明しましたが、歯周病で問題となる歯肉の中の歯周ポケット内部に存在するデンタルプラークの中に生息する細菌のほとんどは、嫌気性菌なのです。
嫌気性菌が歯周病の原因となるのです。

歯周ポケットについて分からない方は以下のページをご覧になって下さい。 歯周ポケット検査(歯周病の基本的な検査)
つまり歯周ポケットの内部には酸素が嫌いな嫌気性菌が生息しているのです。
「歯周ポケットの中は酸素がないの?」
ということですが、
歯周ポケット内部の酸素濃度は1%以下です。(ちなみに私達が生活する空気中の酸素濃度は21%です)
歯周ポケットは、酸素が嫌いな嫌気性菌(歯周病にとって悪い菌)にとってはとても住み心地が良い場所なのです。
喫煙者は、非喫煙者と比較して、歯周病の進行は6倍以上も早いという論文データがあります。
この理由(原因)の一つとして喫煙者の歯周ポケット内部の酸素濃度は正常状態(非喫煙者)の半分程度というデータからも喫煙者は嫌気性菌が繁殖しやすい環境であることが分かります。
5. 細菌の栄養源
口腔内の細菌はなにを栄養源として生きているのでしょうか?
口腔内細菌が必要とする栄養源は、細菌の種類により非常に複雑なものがあります。
私達が口腔内に見える汚れを「歯肉縁上プラーク」と言います。
それに対し、歯周ポケット内部に存在する汚れを「歯肉縁下プラーク」と言います。
口腔内に見える汚れの中に生息する細菌(歯肉縁上プラーク細菌)の主な栄養源は唾液中のアミノ酸です。
歯肉縁上プラーク細菌とは、好気性菌のことです。
酸素が存在する部位でのみ生きることが可能な細菌ですね。
また、好気性菌は、唾液以外にも食物と共に取り込むショ糖やブドウ糖、果糖を利用する細菌も多く存在します。
決して細菌(好気性菌の多くは)は、食物を栄養源としているのではないのです。
主な栄養源は唾液なのです。
しかし、唾液中には抗菌性物質が存在しており、唾液は細菌を殺す働きもあるのです。
唾液は細菌を退治する非常に重要な面(抗菌性)を持っていると共に唾液中のアミノ酸は、細菌の栄養源ともなっているのです。
それに対して歯周ポケット内部に生息する細菌(歯肉縁下プラーク細菌:嫌気性菌)の主な栄養源は歯肉溝滲出液(しにくこうしんしゅつえき)のアミノ酸です。 ※Goodson J M:Periodontol 2000,1994
歯肉溝滲出液とは、歯周ポケット内部からでる液体のことです。
正常状態では、歯周ポケット内部を1分で満たす程度の割合で分泌されています。
歯肉溝滲出液は、単に嫌気性菌の栄養源になっているだけではありません。
歯肉溝滲出液は、歯周ポケット内部に侵入してきた細菌を洗い流す働きがあります。
また、この歯肉溝滲出液には、細菌を撃退する成分(抗菌成分)も含まれています。
例えて言うと、鼻の穴の中に外来から侵入してきた物に対して、鼻汁が出て洗い流したり、目にゴミが入った場合には、涙が出て洗い流すのと同じようなことです。
生体の防御反応といってもいいでしょう。
しかし、この防御としての歯肉溝滲出液は、細菌の栄養源ともなるのです。
また、細菌の中には、他の細菌が出す代謝産物である乳酸を利用するものもあります。
もちろん歯周ポケット内部の細菌とは、酸素が嫌いな嫌気性菌(歯周病にとって悪い菌)のことです。
6. 細菌の成り立ち
口腔内細菌は、単独で悪さをするというよりは、集団で悪さをします。
この細菌の集団をバイオフィルムと言います。
それではバイオフィルムの成り立ちについて解説します。
歯の表面(歯根面)には、ペリクル(唾液の糖タンパク質)という薄い膜が存在します。
※ Marsh P D,et al:J Ind Microbiol,1995
これは、細菌(好気性菌)が出す酸(乳酸)から歯を守る重要な働きをしているのです。
虫歯細菌(好気性菌)は、酸(乳酸)という歯を溶かす成分を出します。
酸(乳酸)より歯が溶けていくのです。
ペリクルは、虫歯細菌による酸から歯を守るバリアーと思って下さい。
しかし、バリアーである反面細菌が付着しやすくなっているのも事実です。
また、歯肉縁上プラーク細菌(好気性菌)の中には食物中のショ糖から粘液性多糖体(水不溶性グルカン)を作るものが多くあります。
口腔内細菌の中には、細菌自体が歯面に付着しやすい構造(線毛等)を持っているものもありますが、歯面に付着しにくい細菌は粘液性多糖体(水不溶性グルカン)を介して凝集していきます。
また、細菌同士が情報伝達を行い、細菌が凝集するのです。
細菌同士が手に手をとって集まる状態を共凝集と言います。
まとめると以下のようになります。
歯の表面(歯根面)には、ペリクル(唾液の糖タンパク質)という薄い膜が形成されます。
このペリクルに付着しやすい細菌(好気性菌 Streptococcus、 Actinomyces)が住みつきます。
この時の細菌(好気性菌)は、歯周病にとって悪性度の低い菌と思って下さい。
さらに この細菌(好気性菌)に嫌気性菌( Fusobacterium nucleatum )が付着します。
※ Kolenbrander P E:J Applied Bacteriol,1993
この細菌( 嫌気性菌:Fusobacterium nucleatum )に歯周病に悪性度の高い細菌
Pg 菌 : Porphyromonas gingivalis
Tf 菌 : Tannerella forsythia
Td 菌 : Treponema denticola
が付着していきます。
※ Socransky S S,et al:J Clin Periodontol,1998
善玉菌、仲介菌、悪玉菌の順番に共凝集していくのです。
こうして細菌の塊ができていくのです。
細菌が集まった状態をバイオフィルムと言います。
※ 細菌の名称は良く変わります 上記は2011年時点での名称です。
7. バイオフィルムは細菌の集合体
多くの細菌が集まった状態をバイオフィルムと言います。
※ Donlan R M,et al:Clin Microbiol Rev,2002
バイオフィルムを他の例えで表現すると台所のシンクをきれいに洗っていないと「ヌルヌル ヌメヌメ」としてきます。
この「ヌルヌル ヌメヌメ」がバイオフィルムなのです。
バイオフィルムは細菌の住処です。バリアーと言ってもいいでしょう。
このバイオフィルムがあると外来からの影響を受けにくくなります。
通常口腔内細菌が繁殖すると 唾液により洗い流されたり、唾液の抗菌作用により細菌が繁殖するのが抑えられます。
しかし、バイオフィルムの中に生息する細菌は、唾液の影響を受けにくくなるためバイオフィルムの中で細菌は増殖していくのです。
飲食後(食物を摂取後) 虫歯細菌(好気性菌)の一部は、多くの糖(ショ糖)から酸(乳酸)という歯を溶かす成分をつくります。
バイオフィルムというバリアで囲まれた中に生息する細菌は、産生した酸(乳酸)の拡散を防ぎ、唾液に流されないために局所に留まります(停滞する)。
そのため、虫歯予防をするためには、バイオフィルムという細菌の住処を破壊することが重要なのです。簡単に言えば歯磨きを行うことです。
8. 虫歯は夜間作られる
先に虫歯細菌(好気性菌)の一部は、多くの糖(ショ糖)から酸(乳酸)という歯を溶かす成分をつくることを解説しました。
飲食物として糖が供給されなくなると糖(ショ糖)から合成され細菌内に貯蔵した水溶性の粘液性多糖体(グルカン およびフルクタン)を利用し、持続して酸(乳酸)などを産生するため、虫歯(脱灰)が起きてしまいます。
虫歯が夜間作られるというのは、食物がなくなった後でも細菌内に蓄えられた粘液性多糖体をエネルギー源として利用しながら酸(乳酸)を産生し続けるためなのです。
9. 好気性菌から嫌気性菌への変貌 -嫌気性菌はどんどんと増殖していく-
先にも説明しましたように口腔内細菌には、好気性菌(酸素が存在する部位でのみ生きることが可能な細菌)と嫌気性菌(酸素が存在する部位では生きるのが困難な細菌)が存在します。
歯周病細菌として問題なのは、嫌気性菌です。
今までの内容をまとめると細菌の増殖の成り立ちとして歯の表面(歯根面)に付着したペリクル表面に好気性菌が増殖します。
そして、食物のショ糖を利用して粘液性多糖体が作られたり、細菌の繊毛等により細菌が凝集してきます。
そしてバイオフィルムが形成されます。するとバイオフィルム中では、どんどんと嫌気性菌の増殖が多くなってきます。
好気性菌から嫌気性菌への変化です。
また、歯肉の上にプラークが沈着してくると歯肉に炎症(腫れる)が起こります。
歯肉が腫れると歯周ポケット内部から歯肉溝滲出液(しにくこうしんしゅつえき)が大量に分泌されるようになってきます。
嫌気性菌にとって歯肉溝滲出液(アミノ酸)は、栄養源ですから栄養源を得た嫌気性菌はどんどんと増えていきます。
歯周ポケット内部のアミノ酸は、唾液中のアミノ酸より20~25倍多く、歯周病細菌にとっては食事に困らない快適な環境と言えます。
※ Fine D H:Periodontol 2000,1995
また、嫌気性菌により歯周組織は破壊され、歯周ポケットがどんどんと深くなりますので、酸素の嫌いな嫌気性菌にとっては絶好の環境になってくるのです。
細菌の増殖は、十分な栄養があれば、1時間もたたないうちに2倍となります。
10. 歯周病の原因となる代表的な嫌気性菌
慢性歯周炎の原因となる代表的な嫌気性菌には以下の3種類があります。
- Pg 菌 : ポリフィロモナス ジンジバリス菌 (Porphyromonas gingivalis)
- Tf 菌 : タネレーラ フォーサイシア菌 (Tannerella forsythia)
- Td 菌 : トレポネーマ デンティコーラ菌 (Treponema denticola)
※ 細菌の名称は良く変わります。上記は2011年時点での名称です。
これらの嫌気性菌の病原性は毒素によって決まります。この毒素には外毒素と内毒素があります。
外毒素は、細菌の内部から分泌されます。
タンパク質を分解する酵素を産生し、歯周組織を構成するコラーゲン組織を破壊します。
コラーゲン組織が破壊されると歯肉は出血しやすくなります。
外毒素として有名なのが赤痢菌や破傷風菌の神経毒、コレラ菌や大腸菌の腸管毒です。
また内毒素は、細菌の構成成分である外膜です。
以下のような多彩な生理活性があり、さまざまな病原性に関わっています。
- 発熱性
- 血液を凝固させ血管障害を起こす
- 細胞障害作用
- 骨吸収を起こす
- 血液を介して内毒素が侵入くるとShwartzman反応という強い炎症反応がみられる
- 一度に大量の内毒素が入り込むと内毒性のショック死を起こすことがある
上記以外にもまだまださまざまな病原性にかかわっています。
11. 生体の生理的防御
細菌から生体を防御するため機構として主に以下の3つのことが関係しています。
1. 唾液
唾液の重要な作用として以下のことがあります。
a.口腔内に侵入してきた微生物を唾液により洗い流す
b.抗菌性物質により感染防御作用をしている
健康な方であれば、唾液は1日に1~2リットル分泌されています。
2. 歯肉溝滲出液(しにくこうしんしゅつえき)
a.歯周ポケット内部に侵入してきた細菌を洗い流す
b.細菌を撃退する成分(抗菌成分)も含まれる
3. 歯肉上皮
歯肉上皮は細菌の攻撃を受けても新しい細胞供給が非常に早いため、細菌の侵入を食い止めるバリアとして働きます。
12. 生体防御細胞
生体防御細胞は、医療を志す学生にとって必ず学ばなければならないことです。
しかし、これがなかなか難しい話しなのです。
以下では、できるかぎり簡単に説明したいと思います。
歯周病で問題となる嫌気性細菌を犯罪者としましょう。
そして後で説明します好中球やマクロファージを警察官としましょう。
ちなみに好中球やマクロファージは、警視庁(白血球)の一員です。
それでは、犯罪者(嫌気性細菌)と警察官(好中球)の話しの始まりです。
外来から攻撃してくる犯罪者(細菌)に対応して唾液や歯肉溝滲出液、歯肉上皮の作用により防御してきますが、細菌の爆発的な増大等により生体内に侵入してくる犯罪者(細菌)がいます。
この時に始めに働くのが、歯肉線維芽細胞のバリアです。
そして、歯肉組織中にいる警察官(マクロファージ)が犯罪者(細菌)に職務質問(攻撃:貪食)します。マクロファージが細菌を食べる(貪食)のです。
また警察官(マクロファージ)は、犯罪者(細菌)を調べます(食べた細菌を分解、消化)。
そして、犯罪者(細菌)がどんな人物(細菌)であるのかを分析します。
この時の分析に役立つのか犯罪者(細菌)の所持物(内毒素)なのです。
所持物(内毒素)の中にその犯罪者(細菌)の情報が詰まっているのです。
警察官(マクロファージ)が出す情報にすぐ反応するのが、血管内に存在する他の警察官(好中球)です。
警察官(好中球)は、血管内を循環しているのです。
※ 好中球の寿命は数時間しかありませんので、細菌が侵入してくるとすぐに攻撃するのです。
警察官(好中球)は、血管から出て来て犯罪者(細菌)に向かい(走化能)、犯罪者(細菌)を丸ごと取り込み(貪食能)、犯罪者(細菌)を破壊(殺菌能)します。
次に警察官(マクロファージ)は分析結果を刑務所(Tリンパ球)に伝えます。
刑務所(Tリンパ球)は その情報をさらに裁判所(Bリンパ球)に伝えます。
そして、裁判所(Bリンパ球)は、刑期(犯罪歴)をつけるのです(抗体を産生)
Bリンパ球から産生された抗体は、細菌にくっつきます。
裁判所が犯罪歴を犯罪者につけるのです。
抗体がくっついた細菌は、好中球が判別しやすくなります。
犯罪歴がついた犯罪者は警察官が判別しやすくなるのです。
指名手配がついたようなものです。
抗体がついた細菌は好中球が捕らえやすくなり(オプソニン効果)、効率よく細菌に対処できるようになります。
予防接種やワクチンは以下のような仕組みで作用します。
少量の抗原(病原体の特徴)を生体内に入れて、病原体の情報を漏らし、あらかじめ抗体を作っておくことです。
インフルエンザワクチンが時々効果のないことがありますが、これはあらかじめ予想していた情報(抗原:ワクチン)が実際に流行ったインフルエンザとは違ったため、情報(抗体)が役立たなかったということです。
13. 嫌気性菌は口臭の原因となる
嫌気性菌の中には増殖する過程で「硫化水素」や「脂肪酸」を産生します。
これが強い悪臭を放ち、口臭の原因の一つとなっています。
14. バイオフィルムには抗生剤が効かない!?
バイオフィルム内に生息細菌には抗生剤が効きにくいことが分かっています。
この理由として以下のことが考えられます。
1. 抗菌剤の浸透性が低い
2. バイオフィルムの深部では細胞の活動性が低い
3. 細菌自体が抵抗性を獲得している
※ Socransky S,et al:Periodontol 2000,2002
そのため、歯周病で歯肉が腫れている人に単に抗生剤を服用してもこの効果を最大限に発揮することは難しくなります。
バイオフィルムは細菌にとってバリアーですからバイオフィルムを破壊することが重要なのです。
15. 細菌の排除(駆除)方法(バイオフィルムの除去方法)
よく患者様からのご質問で「歯周病にデンタルリンス等の洗口剤は効果がありますか?」と聞かれます。
予防という観点で言えば、効果がないとは言いませんが、バイオフィルムの中に存在する細菌を除去することはできません。
先に説明しましたようにバイオフィルムというバリアに守られている細菌は薬液による効果は、ほとんど認められません。
歯周ポケット内部に侵入した細菌を排除(駆除)する方法は、スケーリング・ルートプレーニング(SRP:scaling and root planning )以外にはないと言ってもいいでしょう。
細菌の住処であるバイオフィルムは機械的に除去することが最も効果があります。
※ Slots J,et al:Periodontol 2000,2002
歯肉縁上にある歯石(バイオフィルム)に対しては、PMTC(Professional mechanical tooth cleaning)に勝るバイオフィルム除去はありません。
そして、スケーリング・ルートプレーニングやPMTC後には患者様ご自身による徹底的な歯磨きが重要です。
※ Lavanchy D,et al:J Clin Periodontol,1987
こうしたことが可能であって始めて抗菌性のある消毒薬や内科的薬物治療(飲み薬による歯周病治療)が有効となります。 ※ Kinane DF:Ann R Australas Coll Dent Surg,2000
歯周ポケット内部に存在する嫌気性菌から内毒素が産生され、それが歯の根(歯根面)に付着しています。
以前は、この歯根面に付着している内毒素を徹底したスケーリング・ルートプレーニング(SRP:scaling and root planning)を行うことにより除去できると考えられて来ました。
簡単に言えば、歯根面を一層削るような行為です。
※ Aleo J et al:J Periodontol,1975
しかし、スケーリング・ルートプレーニング(SRP:scaling and root planning)を行い過ぎると歯根面が削れるため、患者様は冷たい物でしみる(知覚過敏症)ことが多く起こりました。
現在では、嫌気性菌が産生する内毒素は歯根面の表層のみに付着しているだけであり、ブラシのようなもので簡単に除去できるということが分かってきています。
※ Nakib N H,et al:J Periodontol,1982
以下は、スケーリング・ルートプレーニング(SRP:scaling and root planning)を行っている動画(YouTube)です。
16. 歯周病細菌を除去後 どれくらいの期間維持できるのか? -歯周病細菌の再発-
歯周病の治療としてスケーリング・ルートプレーニング(SRP:scaling and root planning)という歯肉の中(下)に存在するバイオフィルムを機械的に除去すると劇的に嫌気性菌は減少します。
しかし、100%の細菌が除去できるわけではないので12~16週後にはもとの菌叢に戻る傾向がみられます。
※ Slots,J.et al:J.Periodontol.,1979
歯周病治療(スケーリング・ルートプレーニング:scaling and root planning)により歯周ポケット内部の嫌気性菌は激減しますが、絶対にゼロになるわけではありません。
そのため、残った嫌気性菌が再度増えていくのです。
また歯周ポケットの外部から新たに感染(侵入)してくることも考えられます。
※ Waerhaug J:J Periodontol 1978
また、使用した歯ブラシに付着して生き残った細菌が再度感染を起こす可能性も指摘されています。
若年期に発症し重篤な骨吸収を起こす侵襲性歯周炎(しんしゅうせいししゅうえん)に関与しているAa菌(Aggregatibacter actinomycetemcomitans )は、歯磨きを行った後に 69%も歯ブラシに付着して残っているという研究データがあります。
また、歯ブラシに残ったAa菌は、24時間後でも23%が生き残っているというのです。
※ Muller HP,et al:J Clin Periodontol,1989
上記のデータは歯磨剤を使用しない状態でブラッシングを行ったデータです。
こう考えれば歯ブラシも決して衛生的ではないですね。
また、歯周病治療(スケーリング・ルートプレーニング:scaling and root planning)は、行う術者によりその能力が変わります。
術者の差による歯周病治療結果に関する研究データは多く存在します。
前歯部において歯周病治療(スケーリング・ルートプレーニング:scaling and root planning)を行った場合、歯周病が中程度(歯周ポケット4~6ミリ)の場合には、歯石の除去率は、歯周病専門医で79%であったのに対して、一般開業医では66%の歯石除去率であった。となっています。
歯周病専門医の方が歯石除去率が高いということです。
次に 歯周病が重度(歯周ポケット6ミリ以上)の場合には、歯石の除去率は、歯周病専門医で81%であったのに対して、一般開業医では34%の歯石除去率でした。
※ Brayer WK,et al:J Periodontol,1989
歯周ポケットが深くなればなる程治療は難しくなるため、歯石の取り残しが多くなるというものです。
つまり、誰が歯周病治療(スケーリング・ルートプレーニング:scaling and root planning )を行うかによっても治療効果が変わってくるのです。
しかし、歯周病専門医が行ったとしても100%無菌にすることは不可能なのです。
※ Fleischer H,et al:J Periodontol.1989
ただし、臨床的には100%無菌にする必要性はありません。
歯周病の進行を臨床的に抑える程度まで細菌数を減少させることが重要なのです。
17. 真菌(カビ)は歯周病の原因なのか?
2001年の朝日新聞に「歯周病に抗カビ剤が有効」という記事が掲載されました。
これは、神奈川県内の歯科医院の先生が歯周病治療に「アンフォテリシンBというポリエン系抗真菌剤を使用したところ歯周病が改善した」という意見を元に掲載された情報です。
この情報により歯周病で悩んでいる患者様や一部の歯科医師が飛びつき一時ブーム(?)となりました。
しかし、当然のことながら科学的根拠はなく、うわさだけが先攻してしまったのです。
日本歯周病学会でも社会的影響が大きいとして、学術的に否定情報をHP等で公開しています。
真菌(カビ)は、正常口腔内でも検出される率が高い真菌です。
しかし、真菌(カビ)は、歯周ポケットの深い部分では検出されることは稀です。
真菌(カビ)は、好気性(酸素のあるもとで生きる)あるいは通性嫌気性(若干の酸素の元もで生息可能)のため、酸素がほとんど存在しない歯周ポケットの深い部分(嫌気性)では生息が難しいのです。
しかし、難治性歯周炎の患者様や糖尿病を伴う歯周病患者様、HIV陽性患者様の歯周ポケットで検出されたというデータがありますが、こうした患者様は免疫能の低下や抗菌剤の使用等により増殖した可能性が高いといえます。(日和見感染)Slots J,et al:Oral Microbiol Immunol,1995
こうした科学的根拠のない治療はかなり多く出回っています。
きちんと注意することが必要です。
18. パーフェクトペリオは歯周病細菌に効果があるのか?
パーフェクトペリオは歯周病細菌に効果があるのか?
抗真菌剤アンフォテリシンBと同様に問題となっているのか「パーフェクトペリオ」というものです。
これもある先生がテレビで宣伝(?)したために、爆発的に広まってしまったことです。
また、誤った情報にも関わらず 歯周病に効く(?)、利益がある(?)と考えた歯科医師が便乗してしまい、多くの患者様に不利益をもたらすことになってしまったのです。
現在でもインターネットで検索すると「パーフェクトペリオ」を宣伝しているHPを多く見かけます。
ここまでの内容を見られた方は、歯周病はバイオフィルムによる感染であることをご理解していただけたと思います。
いくら「パーフェクトペリオ」でうがいをしてもバイオフィルムが破壊されることはありませんし、歯周ポケット内部(歯根面)に付着している歯石が取れることはありません。
歯周病治療の長い歴史の中でも効果的にバイオフィルムを除去するための科学的根拠のある治療方法は、機械的に除去するスケーリング・ルートプレーニング(SRP:scaling and root planning )PMTC(Professional mechanical tooth cleaning)なのです。
19. 口腔細菌による全身疾患
口腔内細菌は、歯周組織(歯周ポケット内部)から血液中に入り込んで循環器障害を起こしたり、細菌が産生する毒素や酵素は臓器が細胞障害をもたらします。
細菌心内膜炎
デンタルプラーク中に最も多く存在するStreptococcus sanguinis は細菌性心内膜炎の患者の患部から高頻度に検出されます。
その侵入菌数は、歯周病が進行すると増えていきます。
デンタルプラーク細菌は、さまざまな部位に付着する能力が強く、バイオフィルムを形成するため、血液中に入り込むと菌血症となり、心内膜に付着してバイオフィルムを形成して心内膜炎を起こします。
糖尿病
Ⅱ型糖尿病の方は、歯周病の発症リスクが2~4倍高いという報告があります。 ※ Emrich LJ,et al:J Periodontol,1991
食事によって吸収された栄養分はグルコースという形で血管内にはいります。
これにより血糖値が高くなります。
この血糖値を下げるのが膵臓から分泌されるインスリンです。
インスリンの作用によりグルコースは肝臓 や 筋肉、脂肪細胞に貯蔵されます。
血糖値が低くなると貯蔵されていたグルコースが血液中に放出されて血糖値を一定に保つのです。
糖尿病(Ⅱ型)の場合、脂肪細胞からでるTNF-αという物質がインスリンの作用を阻害するため、血糖値を一定に保ことができなくなります。
歯周病が進行するとこのTNF-αが大量に分泌されるため 血糖値が安定しなくなるのです。
上記以外にも
- 好中球の機能低下
- 微小血管障害
- コラーゲンの合成抑制
- 歯根膜細胞の機能異常
が考えられています。
逆に歯周病を治すと血糖値が安定するという研究報告もなされています。
※ Grossi SG,et al:J Periodontol,1997
早産(低出生体重児出産)
重度の歯周病に罹患している母親は、歯周病に罹患していない健康は口腔内の母親より7倍以上高い確率で低出生体重児を出産しているという報告があります。 ※ Offenbacher S,et al:J Periodontol,1996
心筋梗塞
口腔内細菌(Streptococcus sanguinis、Porphyromonas gingivalis等)は血小板凝集を引き起こすため、血管内で血栓が形成され、血管が閉塞して血流を阻害して心筋梗塞を引き起こします。
骨粗鬆症(こつそしょうしょう)
歯周病と骨粗鬆症に関する研究は年々増加しています。
骨粗鬆症患者様は、非骨粗鬆症 患者様と比較して 歯周病による骨吸収が増大し、骨密度も低下しているという報告があります。
※ Geurs NC,et al:Periodontol 2000,2003
